Урок 06. Тепловой расчёт камеры. Способ второй — лирический (ч.2)
 Доброго времени суток, дорогие друзья!
Доброго времени суток, дорогие друзья!
В прошлый раз я обещал не затягивать с выходом очередного урока, однако, как это нередко бывает, в самом неожиданном месте возникли трудности. Суть их состоит в том, что методика определения парциальных давлений газов продуктов сгорания оказалось неуниверсальной. Если говорить более конкретно, то при определённых комбинациях массовых долей элементов, метод последовательных приближений, описанный ниже, теряет сходимость. На осмысление этого факта ушло некоторое время. Исходные данные, которые мы с Вами использовали (НДМГ + АТ, αок = 0,91), как раз и попали в эту область. Путём подбора было выявлено, что для данной топливной пары метод начинает работать при αок < 0,8. Причины такого поведения алгоритма, скорее всего, кроются в методике выбора и вычисления промежуточных коэффициентов.
Несмотря на обнаруженный недостаток, считаю, что изучение данного метода решения системы имеет определённую пользу с точки зрения понимания сущности теплового расчёта. Поэтому вместо αок = 0,91 зададим αок = 0,8 и пересчитаем массовые доли и энтальпию топлива. Новые значения будут такими: gCт = 0,116; gNт = 0,351; gHт = 0,038; gOт = 0,495; Iп т = 92,5 кДж/кг.
Рассмотрим первый вариант определения парциальных давлений газов в продуктах сгорания азотсодержащего топлива.
Определяем расчётные постоянные Q, R, S:
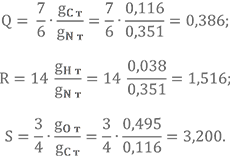
Решение системы выполняем для трёх значений температуры в камере сгорания Tк, кратных 100 К. Значения выбираем в районе ожидаемой Tк. Ожидаемые значения можно выбрать на основе уже известных данных для различных топливных пар, например из таблицы характеристик топлив. Если Вашей топливной пары не нашлось в таблице, не отчаивайтесь, можно взять похожее топливо и отталкиваться от его параметров.
Определяем парциальные давления основных газов продуктов сгорания в первом приближении без учёта газов диссоциации:
![]()
Промежуточные расчётные коэффициенты:
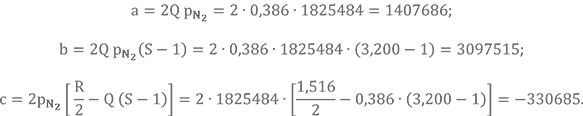
Проверка:
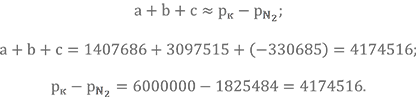
Проверка сошлась, движемся дальше.
Ещё несколько промежуточных параметров для решения квадратного уравнения относительно pCO2 с использованием константы равновесия водяного газа.
![]()
Значение константы К2а выбираем из таблицы констант равновесия для первой точки в окрестности ожидаемой температуры Тк = 3300 К.
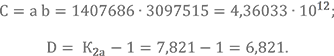
Из двух корней уравнения выбираем положительный, который обычно соответствует приведенной ниже формуле
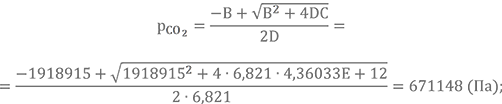
Вычисляем парциальные давления остальных газов в константе К2а:
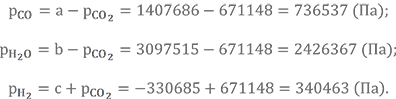
Делаем проверку по двум параметрам:
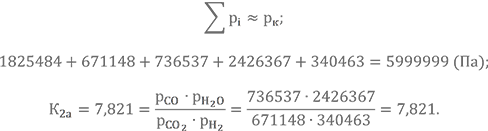
Проверка успешна.
Парциальные давления основных газов в первом приближении определены.
Далее определяем парциальные давления молекулярного кислорода и продуктов диссоциации. Значения констант равновесия берём всё в той же таблице.

Для компактности записи введём ещё несколько дополнительных расчётных коэффициентов:
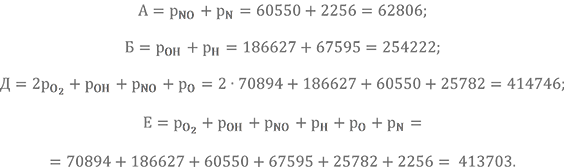
Рассчитываем парциальные давления основных газов с учётом продуктов диссоциации
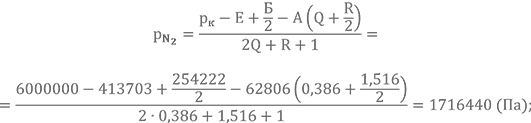
Записываем выражения для определения парциальных давлений основных газов второго приближения
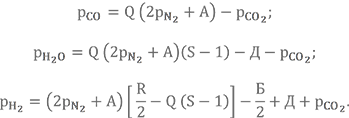
Отсюда получаем новые значения коэффициентов a, b и c
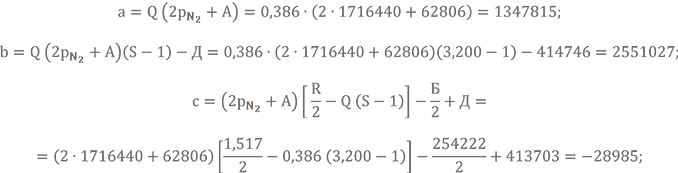
Промежуточная проверка
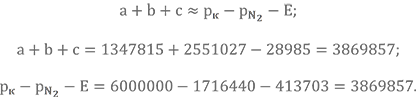
Проверка удалась.
Далее вычисляем новые значения коэффициентов B, C и D для решения квадратного уравнения относительно pCO2, а также парциальные давления второго приближения остальных газов pCO, pH2O и pH2. Выполняем промежуточную проверку и определяем погрешность вычисления парциальных давлений по формуле:
![]()
Проверяем константу равновесия К2а, которая должна совпадать с табличным значением с точностью до четвертой значащей цифры.
Аналогичный расчёт проводим ещё для двух температур. В нашем случае это 3400 К и 3500 К. Обратите внимание, что с увеличением температуры количество итераций заметно увеличивается.
Для автоматизации процесса можно воспользоваться приложением MS Excel, где, например, в столбец таблицы заложить алгоритм расчёта, а затем путём копирования алгоритма в следующие столбцы довольно быстро провести необходимое количество итераций до обеспечения необходимого уровня погрешностей.
Пример такого расчёта Вы можете посмотреть на скриншоте, а сам файл взять .
Для удобства значения парциальных давлений, рассчитанные для трёх температур запишем в таблицу.
| Т, К | p, Па | ||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|
| pN2 | pCO2 | pCO | pH2 | pH2O | pOH | pNO | pH | pO2 | pO | pN | |
| 3300 | 1743343 | 548601 | 813538 | 408749 | 2155747 | 151658 | 43949 | 73968 | 39096 | 19146 | 2205 |
| 3400 | 1715918 | 504702 | 841752 | 434086 | 2066819 | 193624 | 57076 | 97525 | 55308 | 29942 | 3248 |
| 3500 | 1684124 | 457183 | 870825 | 464446 | 1962376 | 239557 | 71395 | 127244 | 73500 | 44680 | 4672 |
Ну что ж, начало положено. В следующем уроке мы с Вами рассмотрим вариант расчёта парциальных давлений газов для топлив, не содержащих азота.
Если Вы считаете, что информация, расположенная на нашем ресурсе, оказалась для Вас полезной, не сочтите за труд рассказать о нас своим друзьям, знакомым и коллегам. Кроме того, Вы можете понажимать на соответствующие разноцветные кнопочки, чтобы популяризовать наш сайт в социальных сетях. Спасибо!
Всем удачи! И до встречи в следующем уроке.
| « | Урок 05. Тепловой расчёт камеры. Способ второй — лирический (ч.1) | Урок 07. Тепловой расчёт камеры. Способ второй — лирический (ч.3) | » |


