Урок 10. Тепловой расчёт камеры. Способ второй — лирический (ч.6)
 Всех приветствую!
Всех приветствую!
У нас очередной урок, посвященный расчёту камеры ЖРД, и мы всё ещё занимаемся тепловым расчётом. Сегодня, наконец, переходим к срезу сопла.
Параметры газа в этом сечении рассчитываются в предположении, что продукты реакций диссоциации и непрореагировавший кислород здесь отсутствуют, поэтому их парциальные давления равны нулю. Таким образом, наша исходная система уравнений существенно упрощается. Однако, как и в случае с камерой сгорания, нам заранее неизвестна температура газов на выходе из сопла.
Схема решения остаётся той же. Выбираем три значения температуры в районе ожидаемой, для которых считаем парциальные давления, энтальпию, энтропию, молярную массу, газовую постоянную. Ожидаемое значение температуры вычисляем по хорошо известной из термодинамики формуле
![]()
Значение показателя изоэнтропы nиз в первом приближении возьмём из таблицы характеристик топлив. Также считаем, что давление на срезе сопла pa задано условием задачи, либо мы выбираем его самостоятельно, исходя из назначения ДУ.
До сей поры мы с Вами как-то ещё не задумывались над значением этого параметра, видимо самое время. Давайте для определённости зададим pa = 0,008 МПа. Показатель изоэнтропы для топливной пары НДМГ + АТ согласно указанной выше таблице — 1,156. Вычислим ожидаемую температуру
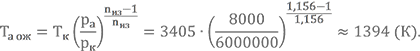
Соответственно выберем три температуры в окрестности этого значения, например, 1300, 1400, 1500 К, и определим в 1-м приближении состав ПС для них.
Для этого используем уже известные формулы (см. Урок 6).
Постоянные Q, R, S пересчитывать не надо, но помним, что pΣ = pa.
Определяем pN2.
![]()
Промежуточные расчётные коэффициенты:
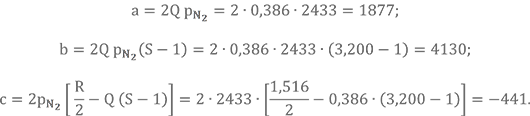
Далее вычисляем параметр B. Причём не забываем, что значение константы К2а нужно выбирать из таблицы констант равновесия для соответствующей температуры. Начнём с 1400 К, К2а = 2,266.
![]()
Также понадобятся промежуточные коэффициенты C и D.
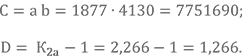
Определяем pCO2
![]()
а также остальные парциальные давления, входящие в К2а
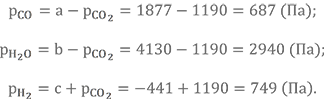
Делаем проверку
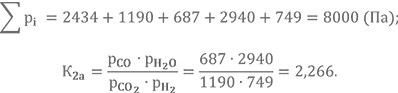
Проверка сошлась.
Теперь я бы рекомендовал сразу вычислить энтропию для только что определённого состава продуктов сгорания (ПС), чтобы посмотреть насколько точно мы угадали с ожидаемой температурой. Рассчитываем её по уже известным из Урока 9 формулам.
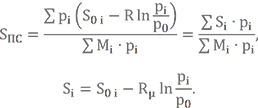
Значения энтропии составляющих газов выбираем из уже знакомого раздела.
Т = 1400 К
| CO₂ | H₂O | CO | H₂ | N₂ | ||
|---|---|---|---|---|---|---|
| Mi , кг кмоль |
44 | 18 | 28 | 2 | 28 | |
| pi , Па | 1190 | 2940 | 687 | 749 | 2434 | ∑pi = 8000 Па |
| Mi·pi | 52358 | 52921 | 19235 | 1498 | 68152 | ∑Mi·pi = 194164 |
| S0i , кДж кмоль·K |
288,3 | 247,5 | 246,4 | 176,7 | 239,5 | |
| Si·pi | 387032 | 814196 | 197790 | 162915 | 658400 | ∑Si·pi = 2220333 |
![]()
Полученное значение, казалось бы, не очень отличается от полученного для камеры сгорания Sк = 11,18 кДж/(кг·К), однако, учитывая, что при разбросе температур от 3300 до 3500 К энтропия изменяется приблизительно на 0,3 кДж/(кг·К), с температурой мы угадали мягко говоря не очень. 🙂 Причём ошиблись в большую сторону. Сказывается выбор показателя изоэнтропы практически наобум. Поэтому предлагаю перезадать ожидаемую температуру. Для грубой прикидки можно заметить, что при изменении температуры газовой смеси на 100 К энтропия изменяется приблизительно на 0,15 кДж/(кг·К). Т.е. температуру продуктов сгорания на срезе сопла можно ожидать где-то в районе 1200К. Зададим три точки в окрестности этого значения — 1100, 1200, 1300 К.
Повторим проделанные выше вычисления, но для новых температур. Результаты занесём в таблицу.
| Ta, К | К2а | pN2, Па | pCO2, Па | pH2O, Па | pСO, Па | pH2, Па |
|---|---|---|---|---|---|---|
| 1100 | 1,056 | 2434 | 1380 | 2750 | 497 | 939 |
| 1200 | 1,432 | 2434 | 1305 | 2825 | 572 | 864 |
| 1300 | 1,840 | 2434 | 1242 | 2888 | 635 | 801 |
Для полученных составов ПС определим соответственно энтальпию, молярную массу и энтропию продуктов сгорания. Ничего нового в вычислениях нет, поэтому приведу только результирующие таблицы.
Т1 = 1100 К
| CO₂ | H₂O | CO | H₂ | N₂ | ||
|---|---|---|---|---|---|---|
| Mi , кг кмоль |
44 | 18 | 28 | 2 | 28 | |
| pi , Па |
1380 | 2750 | 497 | 939 | 2434 | ∑pi = 8000 Па |
| Mi·pi | 60705 | 49507 | 13923 | 1877 | 68152 | ∑Mi·pi = 194164 |
| Iп i , МДж кмоль |
-354,7 | -211,5 | -85,4 | 23,9 | 24,9 | |
| Iп i·pi | -489362 | -581703 | -42481 | 22417 | 60655 | ∑Iп i·pi = -1030474 |
| S0i , кДж кмоль·K |
274,6 | 236,9 | 238,1 | 169,1 | 231,4 | |
| Si·pi | 428135 | 734033 | 140380 | 195279 | 638685 | ∑Si·pi = 2136511 |
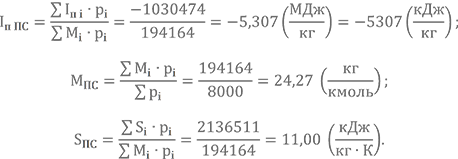
Т₂ = 1200 К
| CO₂ | H₂O | CO | H₂ | N₂ | ||
|---|---|---|---|---|---|---|
| Mi , кг кмоль |
44 | 18 | 28 | 2 | 28 | |
| pi , Па |
1305 | 2825 | 572 | 864 | 2434 | ∑pi = 8000 Па |
| Mi·pi | 57426 | 50848 | 16010 | 1728 | 68152 | ∑Mi·pi = 194164 |
| Iп i , МДж кмоль |
-349,1 | -207,2 | -82,0 | 27,0 | 28,3 | |
| Iп i·pi | -455624 | -585316 | -46903 | 23300 | 68834 | ∑Iп i·pi = -995709 |
| S0i , кДж кмоль·K |
279,5 | 240,6 | 241,1 | 171,8 | 234,3 | |
| Si·pi | 412010 | 763744 | 162467 | 182706 | 645743 | ∑Si·pi = 2166669 |
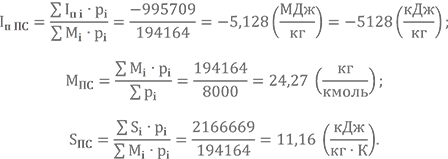
Т3 = 1300 К
| CO₂ | H₂O | CO | H₂ | N₂ | ||
|---|---|---|---|---|---|---|
| Mi , кг кмоль |
44 | 18 | 28 | 2 | 28 | |
| pi , Па |
1242 | 2888 | 635 | 801 | 2434 | ∑pi = 8000 Па |
| Mi·pi | 54666 | 51977 | 17766 | 1603 | 68152 | ∑Mi·pi = 194164 |
| Iп i , МДж кмоль |
-343,4 | -202,7 | -78,6 | 30,1 | 31,7 | |
| Iп i·pi | -426641 | -585320 | -49866 | 24109 | 77085 | ∑Iп i·pi = -960634 |
| S0i , кДж кмоль·K |
284,0 | 244,1 | 243,8 | 174,3 | 237,0 | |
| Si·pi | 398305 | 790284 | 181457 | 171949 | 652315 | ∑Si·pi = 2194310 |
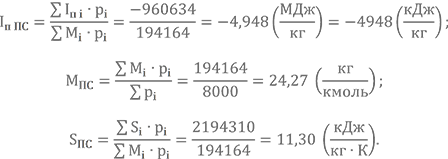
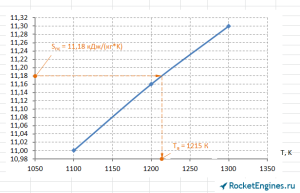
А теперь вспомним об «энергетической связке», о которой я говорил на прошлом уроке. Смысл её заключается в том, что энтропия продуктов сгорания по длине камеры практически не изменяется (почему — вопрос отдельный). Остаётся только, используя это условие, т.е. приравняв значение энтропии в камере сгорания к значению энтропии на срезе сопла, графически определить температуру газов в выходном сечении.
Как видите, получилось приблизительно 1215 К.
Молярная масса, если внимательно посмотреть, не изменяется, т.е. МПС = 24,27 кг/кмоль.
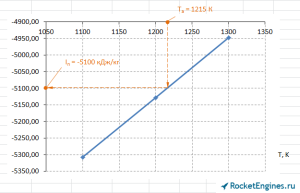
Осталось определить энтальпию — думаю, будет достаточно рисунка.
Iп = -5100 кДж/кг.
И, наконец, газовую постоянную
![]()
Сведём параметры продуктов сгорания на срезе сопла в результирующую таблицу.
| Тa, К | Iп а, кДж/кг | Sa, кДж/(кг·К) | Мa, кг/кмоль | Ra, кДж/(кг·К) |
|---|---|---|---|---|
| 1215 | -5100 | 11,18 | 24,27 | 0,343 |
Что-то опять много букв получилось. 🙂 Особенности расчёта продуктов сгорания, не содержащих азот, оставим на следующий урок.
Подписывайтесь на нашу рассылку, узнавайте первыми о появлении новых материалов на сайте.
Всего наилучшего!
| « | Урок 09. Тепловой расчёт камеры. Способ второй — лирический (ч.5) | Урок 11. Тепловой расчёт камеры. Способ второй — лирический (ч.7) | » |